Riduzione degli odori con
trattamenti aerobici ed anaerobici dei liquami
Andrea Tilche, Fabrizio Malaspina, Loredana Stante
ENEA - Sezione Depurazione e Ciclo
dell’Acqua
Via Martiri di Monte Sole, 4 - 40129 Bologna
Introduzione
I liquami provenienti dagli allevamenti zootecnici e dall’agroindustria contengono sostanze organica sia particolata che disciolta che possono essere fonte direttamente o indirettamente (in seguito all’inizio di fenomeni fermentativi) di cattivi odori (CRPA, 1993). Anche gli impianti di trattamento possono essere fonte di emissioni odorose sgradevoli causati da alcuni sottoprodotti dei processi, in particolar modo per impianti ad alto carico (Anonimo a & b, 1995).
Le elevate cariche microbiche presenti naturalmente in molte tipologie di liquami portano a processi spontanei di degradazione della sostanza organica presente. Nel corso di questo processo si liberano nell’aria composti volatili dotati di attività osmofora (CRPA, 1993). Se tale degradazione avviene in condizioni aerobiche, generalmente gli odori molesti sono irrilevanti; al contrario, se la degradazione avviene in condizioni anaerobiche si libera una vasta gamma di sostanze osmofore anche in elevate concentrazioni (Chiumenti et al., 1991; Sordini et al., 1991). Sono sopratutto i composti ridotti i responsabili dei cattivi odori prodotti dalle strutture di raccolta dei liquami.
Sostanze Osmofore
Le sostanze osmofore liberate dai liquami possono essere raggruppate nella maniera seguente.
— Composti azotati, fra cui la più importante è l’ammoniaca che viene prodotta per deaminazione degli amminoacidi, e le diverse ammine che vengono liberate sopratutto in seguito alla decarbossilazione degli amminoacidi, in particolare durante processi anaerobici a basso pH ed in processi debolmente aerobici (Zender, 1988). Inoltre sono spesso presenti nelle deiezioni anche indolo e scatolo (Ramadori & Tandoi., 1993). Tali composti sono relativamente stabili in condizioni anaerobiche, mentre in condizioni aerobiche si ossidano nelle rispettive aldeidi instabili e tossiche che reagiscono dando composti maleodoranti. Un gruppo di composti azotati osmofori molto offensivi e talvolta anche tossici è rappresentato da alcune ammine primarie, quali ad esempio la cadaverina e la putrescina, che hanno origine dalla decarbossilazione in condizione di limitata disponibilità di ossigeno di aminoacidi. Queste amine risultano relativamente stabili in condizioni anaerobiche, mentre vengono degradate in condizioni aerobiche. In assenza di ossigeno, in condizioni di processo particolari e non usuali si può avere una deaminazione riduttiva che porta alla formazione di acidi volatili. Una deaminazione ossidativa può avvenire in condizioni sintrofiche durante la metanogenesi, ma i primi prodotti di ossidazione possono dare luogo ad altri composti osmofori, quali mercaptani. Inoltre, in presenza di forti concentrazioni di ammoniaca, si può avere una ri-formazione di amine. I composti osmofori di tipo azotato sono frequenti in liquami molto ricchi in materiali proteici come i liquami di allevamenti zootecnici intensivi e i reflui di industrie di lavorazione della carne e del pesce.
— I solfuri provengono dalla degradazione degli amminoacidi solforati (cisteina e metionina) presenti nelle proteine e dal metabolismo anaerobico di batteri solfatoriduttori che utilizzano i solfati come accettori di elettroni. Altri composti organici solforati (mercaptani, alchilsolfuri) possono formarsi dalla degradazione incompleta di composti organici che contengono zolfo, compresi gli amminoacidi (anonimo a, 1995; Zender, 1988).
— Composti ternari, quali acidi organici, aldeidi, chetoni, etc., che si formano dalla degradazione della sostanza organica per vie fermentative. In particolare gli acidi grassi volatili a catena corta si formano normalmente durante la degradazione anaerobica della sostanza organica e a loro volta servono quale substrato per le fasi successive di metanogenesi (e/o di solfatoriduzione) (Zender, 1988). In processi anaerobici, questi acidi possono permanere come residuo nei liquami in concentrazioni tali da essere fonte di odori molesti (limite indicativo di accettabilità 230 mg·l-1 e limite minimo di inacettabilità 650 mg·l-1) (Chiumenti e Donantoni, 1991). Il livello di molestia degli acidi grassi volatili dipende sia dalla volatilità, sia dal numero di atomi di carbonio; gli acidi più volatili sono quelli meno offensivi, mentre i più offensivi - quali ad esempio l’acido valerico (C5) e capronico (C6) - sono relativamente meno volatili.
Le sostanze sopraindicate qualora presenti in aria anche a bassissime concentrazioni (a livello di ppb) sono fonti di odori inaccettabili sia per gli operatori dei sistemi di raccolta e trattamento, sia per le vicine comunità (anonimo a e b, 1995; Chiumenti e Donantoni, 1991).
La soglia odorosa di alcuni composti presenti o liberati dai liquami sono riportati in Tab.1 assieme a valori indicativi di basso ed alto inquinamento (anonimo a, 1995).
TAB. 1. Concentrazioni di soglia in aria per alcuni principali agenti osmofori.
|
Composto |
Concentrazione di soglia |
Conc. di leggero inquinamento |
Conc. di forte inquinamento |
|
|
mg·Nm-3 |
mg·Nm-3 |
mg·Nm-3 |
|
Idrogeno solforato |
0.1 |
4 |
10 |
|
Solfuri totali |
0.15 |
- |
- |
|
Mercaptani totali |
0.07 |
1 |
6 |
|
Ammoniaca |
5 |
10 |
20 |
|
Composti amminici |
0.1 |
1 |
4 |
Processi di trattamento
I processi di trattamento biologico sono in grado di abbattere le emissioni di odori. I processi biologici di trattamento possono distinguersi in tre tipi: anaerobici, aerobici ed anossici. Tutti questi sistemi possono rivelarsi idonei per il controllo delle emissioni odorose dei liquami ma in maniera completamente differente.
Non devono tuttavia essere trascurati tutti quegli accorgimenti che permettano di evitare l’emissione nell’ambiente dei composti odorosi. Un primo accorgimento in tal senso è costituito da sistemi di copertura delle vasche di raccolta con strutture in materiale plastico sia di tipo rigido che flessibile, dotati o meno di sistemi di aereazione interna e di sistemi di filtrazione dell’aria esausta. Alcune soluzioni appaiono relativamente economiche e nello stesso tempo efficaci come per esempio semplici teloni in materiale plastico dotati di sistemi di galleggiamento sul liquame per la copertura di vasche di raccolta dei liquami degli allevamenti zootecnici, in grado di trattenere all’interno le sostanze odorose sviluppate dal liquame (CRPA, 1993). Per la sua semplicità ed economicità questo sistema, ampiamente diffuso e collaudato, consente di coprire anche superfici notevoli. Se applicato su vasche di raccolta e stoccaggio dei liquami, rendendo l’ambiente anaerobico questi teloni di copertura sono in grado anche di raccogliere il gas biologico che si produce e di consentire quindi un suo riutilizzo a scopo energetico. È peraltro necessario che nella progettazione di questi sistemi si abbia l’accorgimento di coprire una porzione di vasca almeno corrispondente a 60 giorni di tempo di permanenza idraulica dei liquami - se la vasca opera a temperatura ambiente - così da permettere una degradazione sufficiente degli acidi grassi volatili che si formano durante il processo. Vi sono molti esempi nei quali, per accelerare il processo e renderlo efficiente anche in condizioni invernali, una certa quantità di gas è bruciata per produrre acqua calda da far circolare in una serpentina posta sul fondo della vasca con cui innalzare di qualche grado la temperatura della vasca stessa. In questi casi, è sufficiente prevedere la copertura di una superficie corrispondente a circa 40 giorni di tempo di permanenza idraulico dei liquami per poter avere un effluente sufficientemente deodorizzato.
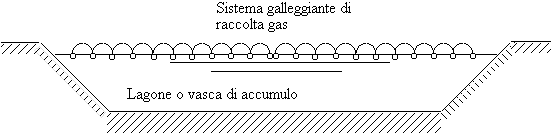
Fig. 1. Sistema di copertura in telone plastico galleggiante.
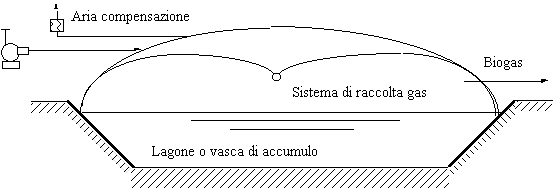
Fig. 2. Sistema di copertura con telone multistrato per raccolta del biogas.
La preventiva rimozione con vagli statici o vibtranti di parte del materiale sospeso evita che tali materiali, di lenta biodegradabilità, che permangono nel liquame, siano substrato per successive fermentazioni e quindi fonti indirette di cattivi odori (Ramadori e Tandoi, 1993).
La Digestione Anaerobica
La digestione anaerobica consiste in una
serie di fermentazioni, catalizzate da specializzati gruppi batterici, che
trasformano il carbonio contenuto nei substrati organici principalmente in due
sostanze gassose monocarboniose, il metano e l’anidride carbonica (Ramadori e
Tandoi, 1993; Zender, 1988).
Nella digestione anaerobica si possono distinguere essenzialmente tre fasi:
idrolisi, fermentazione e metanogenesi. L’idrolisi consiste nella liquefazione
e depolimerizzazione dei substrati complessi, la fermentazione nella loro
conversione principalmente in acidi grassi volatili tra cui acido acetico e la
metanogenesi, infine, nella trasformazione finale di tali substrati in biogas.
Il processo appare molto più complesso in quanto in ogni fase sono coinvolte
più popolazioni batteriche, ognuna delle quali, pur crescendo in stretta
sintrofia con le altre, è impegnata solo in specifici percorsi metaboloci
(Ramadori e Tandoi, 1993; Vismara, 1982; Zender, 1988).
Durante il processo anaerobico si formano normalmente acidi grassi volatili che
vengono poi metabolizzati in acido acetico, idrogeno ed anidride carbonica
(batteri acetogeni), i quali a loro volta vengono utilizzati come substrato dai
batteri metanigeni. In normali condizioni di processo la concentrazione degli
acidi grassi volatili rimane relativamente stabile su valori bassi, in quanto
la produzione di nuovi acidi grassi ad opera dei batteri fermentativi viene
compensata dal consumo degli stessi da parte dei batteri acetogeni e
metanogenici (ed altre comunità, come i solfatoriduttori, se le condizioni del
mezzo lo consente). Tuttavia in particolari condizioni anomale di processo,
come sovraccarichi, presenza di sostanze tossiche, abbassamenti di pH o di
temperatura, si può verificare uno squilibrio tra produzione e consumo degli
acidi grassi volatili: i batteri acetogeni e metanigeni, molto più sensibili
alle condizioni avverse rispetto ai batteri fermentativi, non sono più in grado
di far fronte alla continua produzione di nuovi acidi grassi (Zender, 1988). In
tali condizioni l’equilibrio delle reazioni si sposta e si ha una tendenza
all’accumulo di acidi grassi volatili nel mezzo ed uno spostamento qualitativo
degli stessi verso composti a catena più lunga, che oltre ad inficiare
negativamente sul processo di digestione, sono anche fonte di odori molesti
dell’effluente dove residuano dopo il trattamento. Infatti tali acidi grassi,
dall’odore decisamente molesto, sono estremamente volatili e si liberano
facilmente dalla massa liquida verso l’atmosfera (Chiumenti e Donantoni, 1991;
Zender, 1988).
Durante l’idrolisi e le fermentazioni si formano sostanze osmofore responsabili
dei cattivi odori prodotti dai processi anaerobici non confinati. Inoltre, in
presenza di solfati, si forma idrogeno solforato ad opera di batteri
solfatoriduttori (come il Desulfovibrio,
Desulfobacter e Desulforomonas) (Zender, 1988).
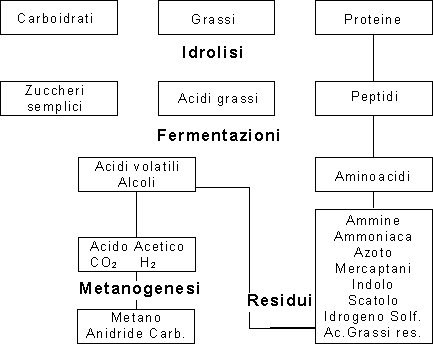
Fig. 3. Schema sintetico del processo anaerobico.
Il trattamento anaerobico dei liquami in condizioni controllate condotto in idonei reattori a tenuta ermetica porta alla degradazione della sostanza organica ed alla stabilizzazione degli effluenti con contemporanea produzione di energia sottoforma di biogas. Il processo, quindi, non porta direttamente alla degradazione dei composti maleodoranti; anzi questi (ammoniaca, ammine, composti solforati, acidi grassi volatili, etc.) si formano in elevate quantità durante il processo, mentre solamente una frazione di queste sostanze (principalmente gli acidi grassi volatili) vengono ulteriormente degradati a composti non odorosi attraverso la metanogenesi. Tuttavia, tali composti osmofori liberati dal processo non vengono rilasciati nell’ambiente ma trattenuti nel biogas recuperato che, per fini energetici, viene bruciato in caldaie o motori endotermici a temperature sufficienti alla loro completa ossidazione chimica in composti non odorosi (CRPA, 1993). Un buon abbattimento degli odori, pressoché completo per quelli più sgradevoli, si può ottenere con impianti nei quali il processo di digestione anaerobica sia condotto a temperature e tempi di ritenzioni adeguati. Inoltre il processo conferisce un certo grado di stabilità anche per i periodi successivi a causa di un rallentamento dei processi degradativi e fermentativi con conseguente diminuzione nella produzione di composti maleodoranti (Ramadori & Tandoi, 1993; Vismara, 1982).
I trattamenti aerobici
Il trattamento di ossidazione biologica è operato da una vasta comunità microbica che cresce aerobicamente degradando gli inquinanti organici presenti nei reflui. Il ruolo primario del processo depurativo è svolto da batteri, sebbene protozoi e piccoli metazoi possono contribuire a determinare la purezza finale dell’effluente per l’opera di predazione dei batteri isolati. Il processo si basa sull’attività di batteri eterotrofi che utilizzano la sostanza organica dei reflui sia per fini strutturali sia per fini energetici. Dalla degradazione della sostanza organica iniziale si ottengono energia e prodotti di ossidazione, quali anidride carbonica ed acqua, e per crescita, nuove cellule batteriche (Ramadori e Tandoi, 1993; Vismara, 1982).
Accanto a queste comunità eterotrofe
possono coesistere comunità di batteri autotrofi in grado di ricavare energia
dall’ossidazione di composti inorganici ridotti, quali ammoniaca e composti
solforati (es. idrogeno solforato).
In particolare batteri come Nitrosomonas
e Nitrobacter ossidano l’azoto ammoniacale ad azoto
nitrico, mentre batteri come Thiobacillus
ossidano l’idrogeno solforato a solfato. Tali microorganismi contribuiscono in
maniera sensibile all’abbattimento degli odori grazie alla rimozione di due
importanti agenti osmofori come l’ammoniaca e l’idrogeno solforato (Ramadori e
Tandoi, 1993; Zender, 1988).
Il trattamento aerobico dei liquami porta
all’ossidazione biologica della sostanza organica limitando in tale maniera la
formazione di quei prodotti della degradazione anaerobica che sono i principali
responsabili dei cattivi odori. Eventuali composti osmofori che si formano
durante il processo vengono in seguito ossidati in composti privi di odori
sgradevoli. Il processo aerobico permette anche il solo controllo degli odori,
senza un’abbattimento spinto della sostanza organica, attraverso l’instaurarsi
di un processo biologico a concentrazioni di ossigeno disciolto nella massa dei
liquami appena superiore allo zero. In quest’ultimo caso tuttavia non si
ottiene una stabilizzazione dei liquami, che riprendono i fenomeni fermentativi
non appena cessano le condizioni aerobiche (CRPA, 1993).
Durante l’ossidazione biologica i composti solforati ed azotati vengono
ossidati rispettivamente a solfati e a nitrati, mentre i composti organici
vengono utilizzati come substrato carbonioso e vengono ossidati ad anidride
carbonica ed acqua. Questa ossidazione spinta richiede impianti adeguatamente
dimensionati con tempi di ossidazione prolungati (Ramadori e Tandoi, 1993;
Vismara, 1982).
In impianti di trattamento ad alto carico possono permanere nel liquame
composti osmofori più resistenti con conseguenti problemi di cattivi odori. I
sistemi impiegati per l’aereazione favoriscono ulteriormente il problema delle
emissioni odorose a causa dell’effetto strippaggio di tali sostanze dal liquame
(anonimo a e b, 1995).
Impianti di trattamento adeguatamente coperti e dotati di un sistema di
ventilazione interno in grado di rimuovere l’aria esausta ricca di composti
osmofori sono un valido ausilio nel controllo delle emissioni odorose. L’aria
esausta può essere sottoposta a trattamenti di tipo biologico per l’ossidazione
dei composti odorosi come per esempio su biofiltri specifici o con sistemi
combinati alla linea trattamento liquame in sezioni a basso carico (per esempio
utilizzando l’aria esausta per aereare un filtro percolatore a basso carico
oppure un cumulo di compost in maturazione ed ancora per l’insufflazione nelle
vasche di ossidazione) (anonimo a e b, 1995).
La Denitrificazione
I processi anossici, cioè processi
ossidativi in cui gli accettori finali di elettroni sono composti inorganici
diversi dall’ossigeno (generalmente nitrato), possono essere utilizzati per la
degradazione ossidativa di sostanze osmofore. I composti solforati ridotti, in
particolare l’idrogeno solforato, possono essere ossidati in solfati dal
batterio chemioautotrofo Thiobacillus
denitrificans utilizzando i nitrati come accettori finali di elettroni che
si riducono ad azoto elementale. Questa reazione avviene in assenza di ossigeno
(che compete col nitrato), in presenza di bicarbonati (fonte di carbonio) e di
azoto ammoniacale (fonte azotata) (Ramadori e Tandoi, 1993; Zender, 1988).
Gli acidi grassi volatili vengono utilizzati come fonte di carbonio per molte
specie di microorganismi eterotrofi che sono in grado di utilizzare i nitrati
come accettori finali di elettroni, qualora essi si trovino in assenza di
ossigeno secondo un processo ampiamente studiato e diffuso utilizzato nei
sistemi di trattamento delle acque per la denitrificazione biologica. Alcuni di
questi microorganismi sono in grado di ossidare in maniera analoga altri
composti osmofori quali le ammine.
Bibliografia
Anonimo, a (1995). Autotrophic biological deodorization of a foul-smelling gases at STPs. World Water and Environmental Engineering, October 1995, pp 28-29.
Anonimo, b (1995). Biological odour control with NTFs. World Water and Environmental Engineering, October 1995, pp 30.
Centro Ricerche Produzioni Animali - CRPA - (1993). Manuale per la gestione e l’utilizzazione agronomica dei reflui zootecnici. Assesorato agricoltura della Regione Emilia Romagna.
Chiumenti R. & Donantoni L. (1991). La stabilizzazione per via aerobica: prove sperimentali su liquami suini. Rivista di Ingegneria Agraria, quad. n. 12, pp 287-301.
Ramadori R. & Tandoi V. (1993). Depurazione biologica delle acque di scarico. In Ecologia Applicata, R. Marchetti ed., Città Studi ediz., Milano.
Sorlini C., Ranalli G. & Andreoni V. (1991). Deiezioni zootecniche e loro trasformazioni: aspetti microbiologici. Rivista di Ingegneria Agraria, quad. n. 12, pp 643-657.
Vismara R. (1982). Depurazione Biologica. Hoepli Editore Milano.
Zhender J.B. (1988). Biology of Anaerobic Microorganisms. Wiley Interscience.